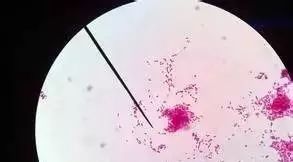
异基因造血干细胞移植后患者腺病毒感染监测及临床意义
-
龙彦 孙媛媛 刘畅 马寅婷 贺春辉 许兰平 赵晓甦 赵晓涛 王辉
选自中华检验医学杂志, 2017,40(02)
人腺病毒(human Adenovirus, HAdv)是一种双链DNA病毒,绝大多数免疫功能正常者在儿童或青少年时均可能感染,常无明显症状或仅表现出轻微的临床症状,如发热、腹泻等。然而,在免疫功能低下人群如HIV感染、实质性器官移植后及异基因造血干细胞移植(hematopoietic stem cell transplantation,allo-HSCT)后患者中,HAdv可再次激活或产生新发感染,甚至发生播散性HAdv感染,引起多器官感染如肠炎、出血性膀胱炎、肝炎及肺炎等,感染率高达3.0%~21.0%[1,2,3],死亡率高达7.7%~38.0%[4],尤其在儿童患者,外周血HAdv高载量和累及多个器官时,死亡率更高。预防性抗病毒治疗或尽早开始抗病毒治疗能降低HAdv感染的临床死亡率。因此,了解allo-HSCT患者HAdv感染的临床特点,早期发现HAdv感染并及时治疗,有助于改善HAdv感染患者的预后。孙于谦等[5]曾对在北京大学人民医院行allo-HSCT后HAdv监测阳性的HAdv感染患者进行了分析,但目前国内尚缺乏HAdv感染的大规模的临床分析数据。本研究通过对北京大学人民医院2012年10月至2014年8月allo-HSCT后患者HAdv感染情况进行分析,为有效监测HAdv感染,指导临床HAdv感染治疗提供一定的实验室依据。
对象与方法
一、对象
病例入选标准:(1)2012年10月至2014年8月在我院进行HAdv监测的allo-HSCT患者;(2)allo-HSCT后自预处理始进行每周2次外周血HAdv监测,直至100 d,临床疑似HAdv感染累及相应器官时,进行相应病灶处标本的HAdv监测,标本类型包括粪便、尿、肺泡灌洗液。100 d后进行必要时监测,包括外周血、粪便、尿、肺泡灌洗液;(3)同时进行巨细胞病毒(Cytomegalovirus,CMV)、EB病毒(Epstein-Barr virus,EBV)的定量监测;(4)随访时间为6个月及以上。本研究通过北京大学人民医院伦理审查委员会审查(批号2013-42),所有患者均签署知情同意书。
二、方法
1.试剂与仪器:
ABI Prime 7300实时荧光定量扩增仪购自美国ABI公司;腺病毒检测试剂盒购自中山大学达安基因公司。
2.标本采集及保存要求:
外周血标本:EDTA抗凝外周血2 ml,标本采集后24 h内低速离心(1 760×g,3 min),分离血浆。非血标本:粪便(>10 g)、尿(>3 ml)、肺泡灌洗液(>3 ml)。分离后的血浆标本3 h内完成核酸提取,外周血分离后血浆或非血标本室温放置不能超过3 h,2~8 ℃保存不能超过1周,-20 ℃保存不能超过1个月。
3.核酸提取:
外周血标本:(1)将已分离好血浆与试剂盒配套核酸提取液按50 μl:50 μl的比例震荡混匀10~15 s,室温放置10~20 min;(3)100 ℃高温裂解10 min;(4)高速低温离心14 000×g 10 min,取上清作为模板进行核酸扩增。非血标本的核酸提取:粪便标本:(1)取2~3 g粪便加适量生理盐水1.0~1.5 ml于1.5 ml离心管中充分混匀洗脱,低速离心(1 760×g,3 min)去沉淀留取上清高速离心(14 000×g,5 min);若为水状便,则直接取1~1.5 ml置离心管高速离心14 000×g 5 min。(2)高速离心后去上清,留取沉淀,再按外周血核酸提取操作步骤(2)~(4)。尿或肺泡灌洗液;直接取标本1~1.5 ml高速离心(14 000×g, 5 min),去上清,留取沉淀,按外周血核酸提取操作步骤(2)~(4)。
4.PCR反应扩增:
按照试剂说明书比例(HAdv PCR反应液38 μl/人份+Taq酶3 μl/人份)配置反应体系,充分混匀后按41 μl/管分至0.2 ml PCR反应管中,然后将提取好的核酸模板上清液、质控品(阴性、弱阳性和强阳性质控)、标准品(S1:2×107、S2:2×106、S3:2×105、S4:2×104)4 μl分别加入配置好的反应体系中,瞬时离心10~15 s混匀,同时将4 μl,加盖密封备用。反应条件:93 ℃ 120 s,93 ℃ 45 s,55 ℃ 60 s,10个循环,93 ℃ 30 s,55 ℃ 45 s,30个循环;选择检测通道为FAM通道。如果扩增曲线不呈S型曲线或循环阈值(cycle threshold,Ct)值=30,则样本检测值小于检测极限,如果扩增曲线呈S型曲线且Ct值<30,则由标准品绘制的标准曲线,得出相应的定量检测值。同时阴性、弱阳性及强阳性质控均应在控。
5.allo-HSCT方案:
详见文献[5]。
6.HAdv感染相关临床疾病定义[6]:
系统性HAdv感染/HAdv血症:应用PCR技术或抗原检测、病毒分离等方法从患者外周血中检出HAdv核酸阳性。局部感染:应用PCR技术或抗原检测、病毒分离等方法从活检组织或体液等中(不包括外周血)检出HAdv核酸阳性。临床诊断HAdv病:HAdv阳性同时伴有相应的临床症状,但无组织病理学证实。确诊HAdv病:HAdv阳性同时伴有相应的临床症状,组织病理学证实HAdv阳性。
结果
一、病例特点
本研究共入选allo-HSCT患者845例,其中男性和女性分别为448和397例,中位年龄为31(1~63)岁,儿童和成人分别为155和690例。同胞相合患者共280例,单倍体相合移植患者共545例,非血缘移植20例。在845例入选人群中,以急性髓系白血病、急性淋巴细胞白血病及骨髓增生异常综合征最多,分别为349、272和112例,其次为慢性髓系白血病、再生障碍性贫血、多发性骨髓瘤及非霍奇金淋巴瘤。
二、HAdv实验室阳性检出率情况分析
本研究共检出HAdv阳性29例,其中男19例、女10例,中位年龄为25(3~57)岁。单倍体相合移植患者共28例,同胞相合1例。在845例入选人群中,急性髓系白血病、急性淋巴细胞白血病及骨髓增生异常综合征,分别为10、10和6例,其他3例分别为非霍奇金淋巴瘤再生障碍性贫血和多发性骨髓瘤;共25例患者在allo-HSCT后发生急性移植物抗宿主病(graft-versus-host disease,GVHD)[(86.2%,25/29)急性GVHD Ⅰ~Ⅱ°14例、急性GVHD Ⅲ~Ⅳ°11例],4例发生慢性GVHD(13.8%, 4/29)。
HAdv检测阳性率为3.4%(29/845),儿童(<18岁)阳性率为3.8%(6/155),成人(≥18岁)阳性率为3.3%(23/690)。allo-HSCT后在100 d内HAdv检出阳性占总阳性例数的72.4%(21/29)。其中外周血HAdv阳性共19例,尿HAdv阳性9例,粪便阳性16例,肺泡灌洗液阳性1例,外周血+粪便HAdv阳性7例,外周血+尿HAdv阳性5例,外周血+肺泡灌洗液HAdv阳性1例,其中外周血+粪便+尿HAdv阳性1例。HAdv检出阳性的中位时间为69(13~189)d;外周血检出阳性的中位时间为85(40~102)d;粪便为56(53~144)d;尿为51(28~81)d。
三、临床HAdv感染合并其他病毒感染情况分析
HAdv检测阳性人群中,17例合并CMV血症(58.6%,17/29),CMV血症发生的中位时间为30(11~135)d,11例合并EBV血症(37.9%,11/29),EBV血症发生的中位时间为43(34~163)d,CMV血症和EBV血症发生的中位时间均早于HAdv。25例HAdv检测阳性前均发生了GVHD,其中累及皮肤18例,肠道16例,肝脏2例,4例发生了GVHD。
四、HAdv临床诊断及转归
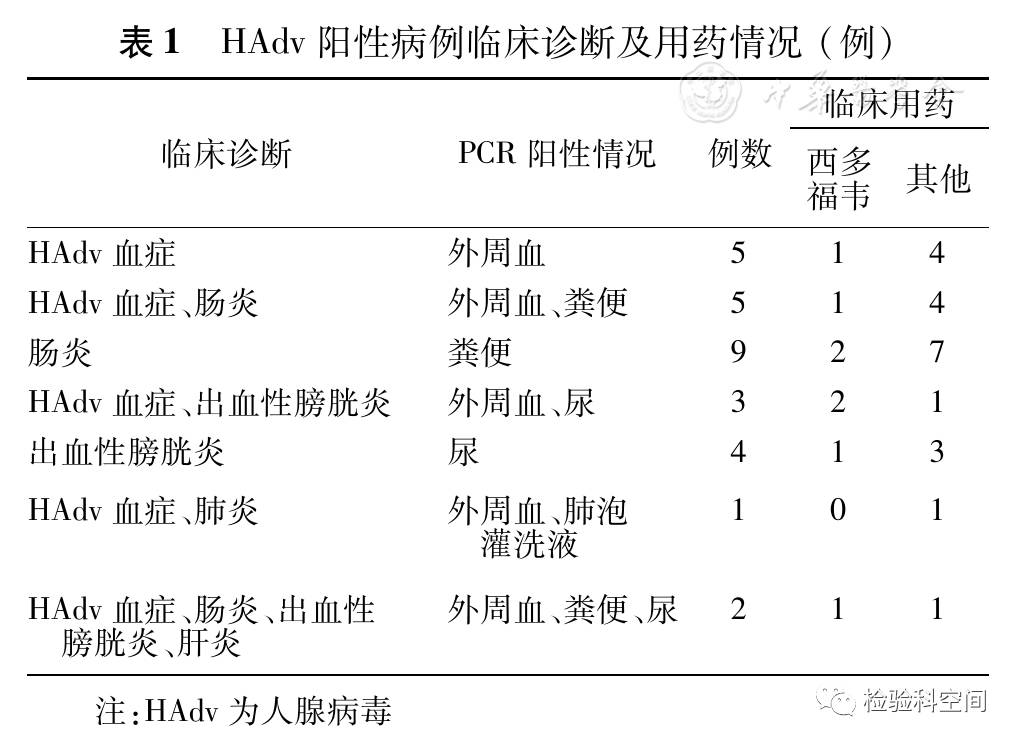
结合HAdv检测结果和临床资料显示,有5例诊断为HAdv血症(外周血HAdv阳性);14例诊断HAdv肠炎(腹泻且粪便HAdv阳性),其中5例为HAdv血症+肠炎,7例诊断为出血性膀胱炎(血尿且尿HAdv阳性),其中3例合并HAdv血症+出血性膀胱炎,2例诊断为HAdv血症+肠炎+出血性膀胱炎+肝炎(肝功能急剧恶化,除外GVHD及药物性肝损害),1例为HAdv血症+肺炎,见表1和图1。8例患者给予西多福韦(每周5 mg/kg)治疗,6例经西多福韦治疗后HAdv转阴,2例经西多福韦治疗无效,见表2。
|
表1 HAdv阳性病例临床诊断及用药情况(例) |
|
表2 8例HAdv感染allo-HSCT患者临床资料 |
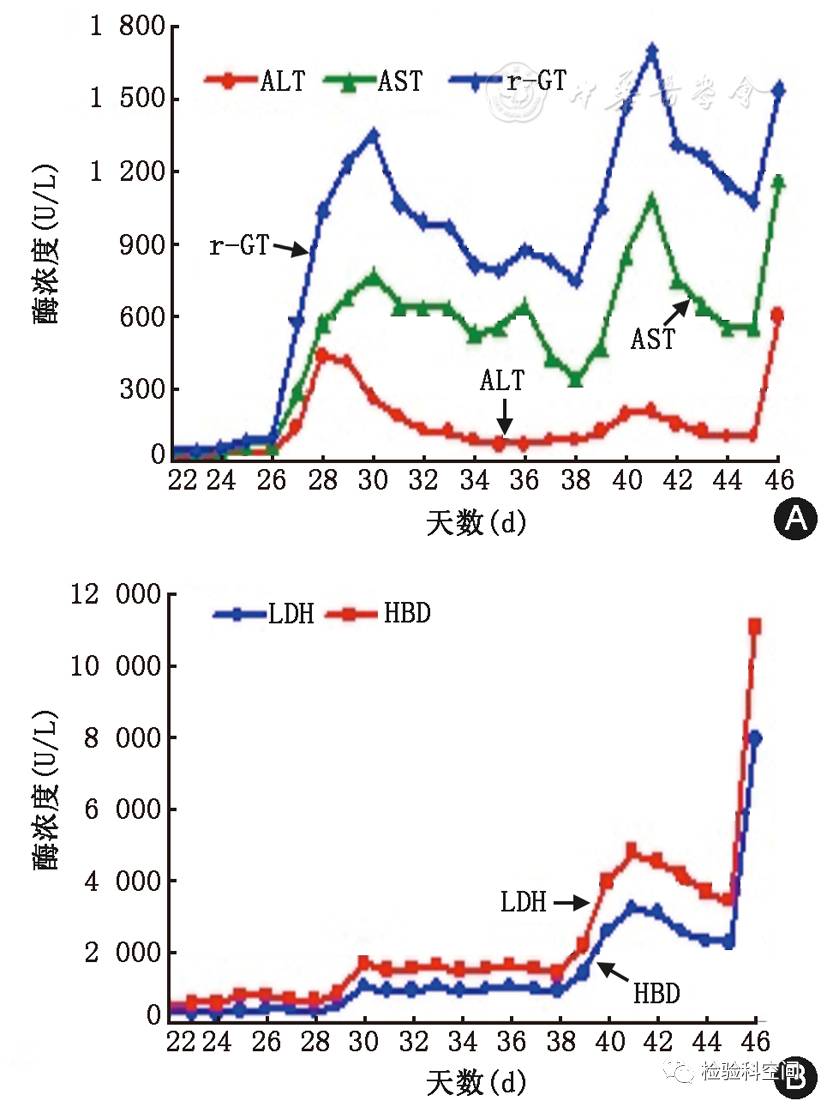
图1
1例HAdv血症+肠炎+出血性膀胱炎+肝炎经西多福韦治疗无效死亡患者肝功能变化
讨论
病毒感染是allo-HSCT后患者常见的严重并发症之一,临床常见病毒有CMV、EBV等。近年来,HAdv的感染率逐年增加,导致患者感染的危险因素主要包括:儿童(<18岁)、去T细胞移植、合并GVHD、单倍体相合移植、脐带血移植、抗胸腺球蛋白(anti-thymoeyte globulin, ATG)治疗及外周血淋巴细胞计数<0.2×109/L等[4]。国外文献报道allo-HSCT后患者HAdv感染率高达3.0%~21%[4,7],儿童感染率为6%~42%[8],成人3%~15%[1,9]。本研究中HAdv感染率为3.4%(29/845),儿童HAdv感染率为3.8%(6/155),高于成人3.3%(23/690),与国外文献报道较为一致,但二者感染率均低于国外报道。分析原因可能为:首先,本研究人群中未纳入脐带血移植患者,均未采用体外去T细胞移植模式。而国外较常采用体外去T细胞移植和脐带血移植,二者均是发生HAdv感染的高危因素。其次,本研究对allo-HSCT后患者外周血、粪便、尿及肺泡灌洗液进行监测,未进行咽拭子、肠黏膜组织等标本检测。另外,本研究患者常规监测至allo-HSCT后100 d,但部分患者在100 d后,由于当地尚未开展HAdv检测,故未能在必要时继续监测,致使这部分患者100 d后发生的HAdv感染未能发现,以上均使得国外文献报道的HAdv感染率较高,此外,本研究感染率高于孙于谦等[5]报道的单倍体移植后100 d ADV血症累积发生率为1.1%,分析主要有两方面的原因:首先,入选人群的差异,本研究除研究在我院行allo-HCST的患者外,尚包括在外院行allo-HSCT后,由于病情较重转入我院进行监测治疗的患者,此部分患者是病毒感染包括HAdv感染的高危人群;此外,孙于谦等[5]分析移植后100 d ADV血症累积发生率,本研究尚对非血标本HAdv监测阳性的患者同时进行分析,同时与临床医生对HAdv感染的警惕性有很大提高,重视对allo-HSCT患者的HAdv监测有关。HAdv感染在儿童患者中更易发生,且发生的时间更早,预后更差,原因可能为儿童尚未建立针对各种血清型HAdv的有效免疫防御机制。此外,本研究HAdv阳性患者中82.7%(24/29)合并GVHD,其中20例合并GVHD,4例合并GVHD,因此,对于儿童患者、合并GVHD人群,应重视HAdv的监测。同时对于单倍体移植人群,在临床高度怀疑HAdv感染时,应及时进行HAdv检测,目前已纳入欧洲白血病感染会议的推荐[6]。
HAdv感染一般发生在allo-HSCT后2~3个月(100 d)内,可累及全身多个脏器,表现为肠炎、出血性膀胱炎、肺炎、肝炎、胰腺炎,甚至脑炎、肾炎等。本研究人群中,临床表现以肠炎48.3%(14/29)和出血性膀胱炎24.1%(7/29)最为常见,2例累及多个脏器,临床诊断为HAdv血症+肠炎+出血性膀胱炎+肝炎,1例患者诊断为HAdv血症+肺炎。大部分患者经抗病毒治疗后,HAdv转阴,但仍有部分患者即使应用西多福韦治疗后,仍未能控制病情,共8例临床死亡,病死率为27.6%(8/29),国外文献报道为7.7%~38.0%[4,10],依据检测结果和临床资料,可能有以下原因导致患者预后差:首先,此8例患者外周血HAdv定量值均>1 000拷贝数/ml,最高达108拷贝数/ml;其次,8例患者中,有6例在allo-HSCT后100 d内发生HAdv感染,仅2例发生在100 d后(分别为183 d,131 d),HAdv感染发生愈早,患者预后愈差,国外文献报道allo-HSCT后100 d内发生HAdv感染,致命性、播散性HAdv感染的发生率>60%[11,12]。再次,累及多个器官(>2个)或累及肺和肝脏时,预后差、死亡率高,国外文献报道高达83%[13]。本研究中2例累及多个器官(>2个)患者和1例累及肺部的患者在随访期内临床死亡。最后,合并其他病毒感染亦是导致患者预后差的原因,其中8例患者均合并CMV感染,5例合并EBV感染。
在本研究入选人群中,有2例患者合并HAdv肝炎,HAdv肝炎临床表现非特异,在HAdv感染累及肝脏2周左右后方可出现肝功能异常,预防性或早期使用西多福韦能使部分患者HAdv转阴,故早期诊断对临床意义重大。本研究中2例患者经影像学检查除外如药物性肝损害等[11],临床诊断为HAdv肝炎,在肝功能异常指标中,转肽酶升高较AST和ALT均较早且升高幅度更大,此前已有类似文献报道[12,13],因此,当临床外周血HAdv阳性同时有肝功能异常时,经影像学检查排除GVHD和药物性肝损伤时,转肽酶升高对HAdv肝炎的早期诊断具有预警作用,提示临床可尽早使用西多福韦进行抗病毒治疗,从而改善患者预后,但本研究中HAdv肝炎患者例数尚少,有待进一步扩大样本量进行验证。
更多精彩尽在中华检验医学杂志