BRAF基因突变肺癌患者的临床特征及结果研究
关键信息:BRAF基因突变NSCLC患者的中位OS为22.1个月,对照组野生型NSCLC患者的中位OS为14.5个月,无统计学差异(p=0.095);BRAF V600E基因突变NSCLC患者的中位OS(25个月)长于BRAF 非V600E突变患者的中位OS(13个月)(p=0.153);IV期 KRAS V600E突变患者的OS(16个月)长于KRAS 非V600E突变患者的OS(7个月),但无显著性差异(p=0.272)。
摘要
简介:非小细胞肺癌(NSCLC)患者中BRAF基因突变比例约为2%。由于该突变较少见,因此目前为止,突变患者相关的临床特征及预后意义均没有详细描述。
方法:2012年2月至2014年10月间,本研究在里昂大学医院实验室利用法国国家癌症研究所对转移性肺癌患者进行系统的分子检测,连续收集含有BRAF基因突变的NSCLC患者的临床特征,并对结果进行了分析。此外,我们与EGFR、BRAF、KRAS、HER2、PIK3CA基因野生型的NSCLC患者进行了变量对比。
结果:本研究中共有2690例NSCLC患者进行了基因分型,BRAF基因突变患者80例(3%),其中42例(53%)是V600E替换突变,38例(48%)不是V600E替换突变。BRAF基因V600E突变患者中未发现其他突变,非V600E突变的BRAF基因突变患者中发现5例患者同时具有KRAS基因突变。V600E突变患者与非V600E突变患者间的年龄、组织类型、体力状态以及诊断分期均没有显著差异。BRAF野生型、V600E BRAF突变、非V600E BRAF突变患者间的总生存期(OS)没有显著差异。
结论:该研究是样本量最大的BRAF基因突变NSCLC患者的研究。临床数据表明,BRAF基因突变是NSCLC患者的特定部分,然而BRAF基因突变,尤其是非V600E BRAF突变在肺癌中的致癌性质仍未确认,BRAF基因突变对靶向药物疗效的预测价值仍未知。
前言
除了EGFR和ALK基因突变,NSCLC患者中也可能存在BRAF基因突变。BRAF是RAS-RAF-MEK-ERK信号通路中位于KRAS下游的丝氨酸/苏氨酸激酶。当BRAF基因发生致癌突变被激活时,会持续磷酸化MEK,并促进细胞的生长、增值及生存。BRAF基因突变常发生于黑色素瘤中,在其他癌症中发生频率远远较低,如乳头状甲状腺癌、直肠癌、卵巢癌以及肺癌,据报道,肺腺癌中BRAF的突变频率只有2%。
之前针对BRAF基因突变NSCLC患者临床特征的研究限于样本量小并且主要集中在V600E突变类型,然而NSCLC肺癌中存在多种其他突变。
本研究分析了BRAF基因突变NSCLC患者的临床特征及结果。对这些变量的深入了解有利于该部分患者的更好管理,同时有利于为患者选择合适的特异性靶向治疗药物。
方法
1.数据收集
本研究中的患者均来源于里昂大学医院的分子诊断实验室数据库,包括2012年2月至2014年10月期间诊断为BRAF基因突变的NSCLC患者。除肺癌标本外其他恶性肿瘤的标本均排除在外。所有患者的BRAF、EGFR、KRAS、HER2、PI3K基因突变以及ALK重排均考虑在内。详细的临床特征包括:吸烟史、职业性接触、病史、体力状态、分期、原发部位、治疗史、RECIST评分以及生存期,通过专业调查问卷直接或间接的收集以上信息。
2.常规突变分析
在法国,无法接受局部治疗的腺癌患者或非其他特殊的癌症患者,以及不吸烟的鳞癌患者均被要求进行EGFR、KRAS、BRAF、HER2基因突变以及ALK重排检测。肿瘤组织标本被切割成小块,以便筛选出肿瘤细胞含量最多且体积最小的肿瘤组织。样本中含有至少75%的肿瘤细胞。使用DNA提取试剂盒(Qiagen, Valencia, CA, USA)提取肿瘤DNA。使用PCR扩增试剂盒(Qiagen, Valencia, CA, USA)扩增BRAF基因的11号外显子和15号外显子。PCR产物使用试剂盒(GE Healthcare Life Sciences,Buckinghamshire, UK)进行纯化。然后对PCR产物进行测序。
3.病例对照分析
为了更好地分析BRAF突变NSCLC患者的临床特征及预后价值,本研究进行了病例对照分析,对照病例均是没有ALK重排突变以及野生型EGFR、KRAS、BRAF、HER2、PIK基因肺癌患者的随机标本。2个对照病例与BRAF突变病例随机配对。
结果
1.BRAF突变发生率
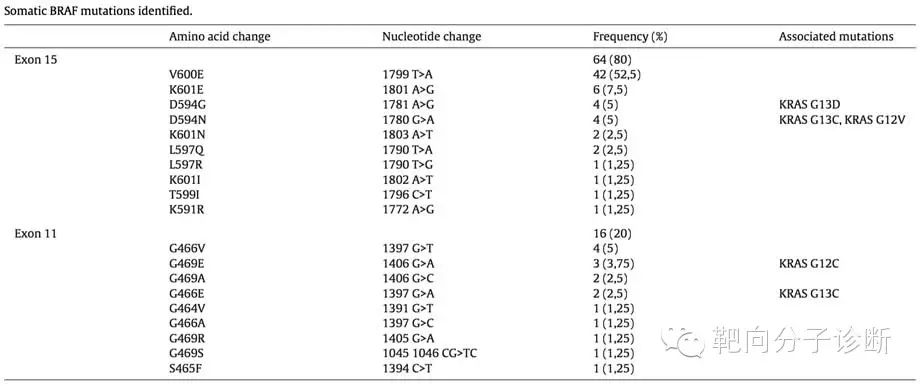
2012年2月至2014年10月间,共分析了来自2690例NSCLC患者的2887个样本的BRAF基因突变状态。共检测到80例(3%)BRAF突变(表1),其中42例(53%)是V600E替换突变,38例(48%)是非V600E突变(表1),这些非V600E突变局限分布在15号外显子的591、594、597、599密码子以及11号外显子的464、465、466及469密码子上。BRAF基因V600E突变患者中未发现其他并存突变,5例BRAF基因非V600E突变患者中检测到KRAS基因突变(表1)。
表1 体细胞BRAF基因突变鉴定
2.患者特征
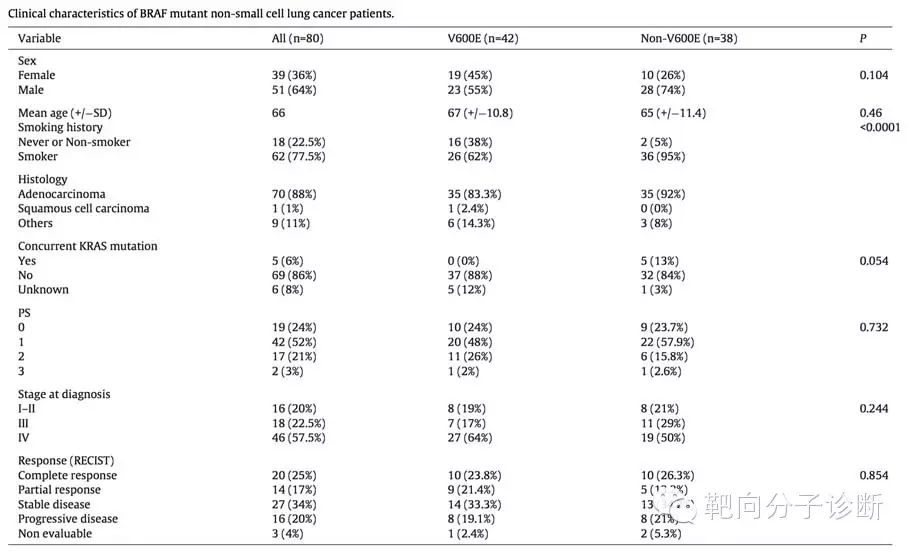
表2详细的总结了患者特征。V600E突变患者和非V600E突变患者间的年龄、组织类型、PS、诊断分期没有显著差异。非V600E突变患者中男性居多,而V600E突变患者中男性较少,但未有显著差异(p=0.104)。大多数BRAF基因突变晚期患者中:46例(57.5%)患者确诊时为IV期。相较于V600E突变患者,非V600E突变患者中有更多的吸烟者(p<0.001)。
肿瘤组织类型以腺癌为主,符合法国NCI项目的临床基因分型部分的人口特征。本研究中没有与V600E或非V600E突变相关的组织学亚型。
非V600E突变患者中吸烟患者比例(95%)尤为显著,V600E突变患者中吸烟者比例(62%)较少(p<0.0001)。
对照组中,性别分配、平均年龄和BRAF突变病例类似,为33%男性和67%女性(p=0.566),平均年龄为65岁(p=0.618),这些结果没有显著性差异。
表2 BRAF基因突变NSCLC患者临床特征
3.特定抑制剂治疗
9例患者(11%)接受了BRAF酪氨酸激酶抑制剂治疗:3例患者接受达拉菲尼治疗,3例患者接受维罗非尼治疗,3例患者接受达拉菲尼和trametanib的联合治疗。5例患者接受BRAF抑制剂二线或三线治疗(1例患者是一线,1例患者是四线,1例患者是五线)。经过19个月的治疗后,9例患者中的6例仍在继续治疗,其余3例患者的总生存时间分别为13个月、13个月和25个月。
4.生存分析和病例对照分析结果
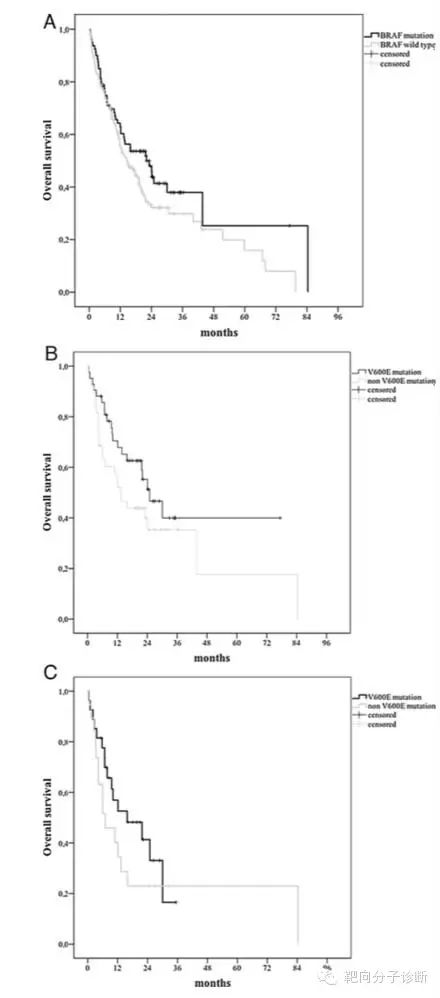
如图1中所示,BRAF基因突变NSCLC患者的中位OS为22.1个月,对照组野生型NSCLC患者的中位OS为14.5个月,该结果无统计学差异(p=0.095)。
BRAF V600E基因突变NSCLC患者的中位OS(25个月)长于BRAF 非V600E突变患者的中位OS(13个月)(p=0.153)。IV期 KRAS V600E突变患者的OS(16个月)长于KRAS 非V600E突变患者的OS(7个月),但没有显著性差异(p=0.272)。
图1 总生存时间比较
结论
本研究是样本量最大的BRAF基因突变NSCLC患者的研究。一半的BRAF突变是非V600E突变,BRAF非V600E突变在吸烟者中更常见,且与KRAS基因突变相关。本研究分析了BRAF基因突变NSCLC患者的临床特征及结果。对这些变量的深入了解有利于该部分患者的更好管理,同时有利于为患者选择合适的特异性靶向治疗药物。
信息来源:
ClaireTissot, Sébastien Couraud, Ronan Tanguy, et al. Clinical characteristics andoutcome of patients with lung cancerharboring BRAF mutations. Lung Cancer 91(2016) 23–28.