单基因突变可显著降低疟疾感染风险
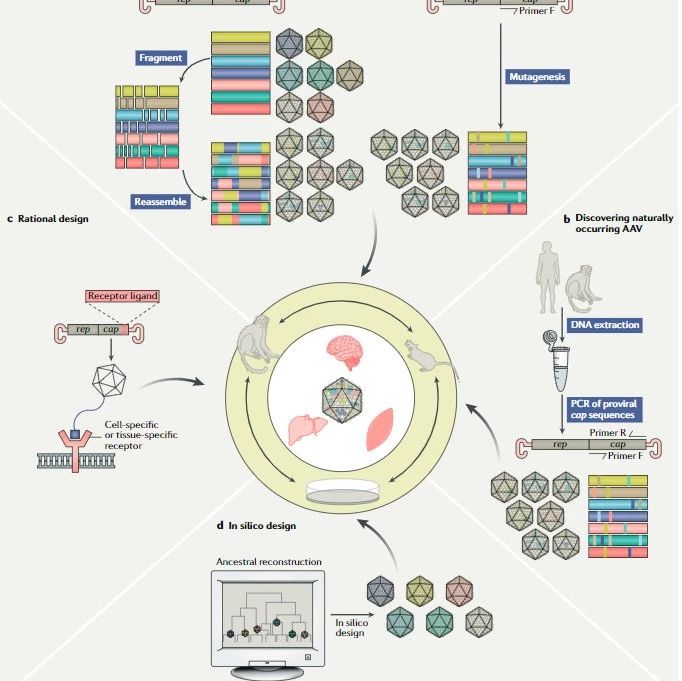
2017年5月18日,Science杂志在线发表了英国牛津大学联合剑桥大学等研究者合作的题为Resistance tomalaria through structural variation of red blood cell invasion receptors的研究成果。研究者对撒哈拉地区几千人进行了全基因组的测序,用于寻找与疟疾有关的血细胞标志物,并发现了一类存在于血红细胞中的单基因的突变可帮助机体抵抗疟疾。该研究有助于人类了解机体抵抗疟疾的作用机理,并为新型疗法的开发提供了思路。
疟疾是由来自疟原虫属的五种单细胞生物感染引发的疾病,可通过蚊子的叮咬传播,并且能够入侵宿主的血红细胞进行增殖。血红细胞快速的生长与增殖使得疾病症状加重,其中包括高烧、流汗、发抖、疼痛以及死亡。
为了进入细胞,疟原虫进化出了许多种识别血红细胞表面受体的方式;此外,疟原虫还能够产生一系列的蛋白由于与靶细胞表面的受体向连接,这些蛋白质也是目前特异性疫苗的研发思路。
为了寻找与疟疾有关的血细胞标志物,研究者对撒哈拉地区数千名患有疟疾的人群以及正常人的基因组进行了测序,并进行了比较,鉴定出了十几种受体蛋白,其中包括决定血型的A.B蛋白。之后,研究者们发现在血型糖蛋白基因的周围出现了多拷贝数的现象,而且复制的区域中出现了27处突变(图1)。
图1 血型糖蛋白的多倍化现象
这些突变主要影响了撒哈拉人群的血细胞表面糖蛋白的构成,其中DUP4的突变伴随着对疟疾疾病的较强抵抗特性,携带该突变的人群患疟疾的几率要比其他人群低40%(图2)。
图2 疟疾患病着中的DUP4突变分析
目前该基因突变对宿主抵抗疟疾感染的影响机制还不清楚,但研究者们认为它可能影响了GYPB-1异源二聚化的形成,进而影响了疟原虫的侵入(图3)。对该基因的进一步认识能够帮助我们提高抵抗疟疾感染的成功率。
图3 DUP4的结构特点分析
疟疾是由疟原虫属寄生虫所致。这些寄生虫通过被称为“疟疾病媒”的受感染雌性按蚊叮咬传至人类。共有5种寄生虫会导致人类疟疾,其中恶性疟原虫和间日疟原虫危害最大。恶性疟原虫是非洲大陆最常见的疟原虫。它导致全球大多数疟疾死亡病例。在撒哈拉以南非洲之外的大多数国家,间日疟原虫是主要的疟疾寄生虫。
症状
疟疾是一种急性发热疾病。对于无免疫力的人而言,会在受到感染的蚊虫叮咬7天或7天之后(一般是10-15天)出现症状。最初症状(发热、头痛、寒战和呕吐)可能较轻,并因此而难以发现是疟疾。如果不在24小时内予以治疗,恶性疟可能发展成严重疾病,并且往往会致命。患有严重疟疾的儿童常常出现以下一种或多种病症:严重贫血,与代谢性酸中毒相关的呼吸窘迫,或脑型疟。成人也频频出现多脏器病症。在疟疾流行地区,人们可能产生局部免疫力,导致出现无症状感染。
谁有风险?
根据WHO报道,2015年,全世界约一半人口面临疟疾风险。多数疟疾病例和死亡发生在撒哈拉以南非洲。然而,东南亚、拉丁美洲以及中东地区也受到影响。2015年,91个国家和地区有持续性的疟疾传播。
一些人群感染疟疾病毒并发展为严重疾病的风险比其他人群高得多。高风险人群包括婴儿,5岁以下儿童,孕妇,艾滋病毒感染者和艾滋病人,以及无免疫力的移民、流动人口和旅客。国家疟疾控制规划需要针对这些人群的具体情况,采取专门措施保护他们免受疟疾感染。
The malariaparasite Plasmodium falciparum invades human red blood cells via interactionsbetween host and parasite surface proteins. By analyzing genome sequence datafrom human populations, including 1269 individuals from sub-Saharan Africa, weidentify a diverse array of large copy number variants affecting the hostinvasion receptor genes GYPA and GYPB. We find that a nearby association with severemalaria is explained by a complex structural rearrangement involving the lossof GYPB and gain of two GYPB-A hybrid genes, which encode a serologicallydistinct blood group antigen known as Dantu. This variant reduces the risk ofsevere malaria by 40% and has recently risen in frequency in parts of Kenya,yet it appears to be absent from west Africa. These findings link structuralvariation of red blood cell invasion receptors with natural resistance tosevere malaria.
原文链接:
Ellen M.Leffleret al.Resistance to malaria through structural variation of red bloodcellinvasion receptors.Science(2017).DOI: 10.1126/science.aam6393
本期编辑:Annabella
★
中国病毒学论坛是一个非盈利性的公益性论坛,致力于共建病毒学研究人员的交流互助平台。秉承“积极交流与分享,携手合作与共赢”的理念,中国病毒学论坛特创办“病毒学界”自媒体,在此向公众征稿,竭诚欢迎病毒学领域研究进展、科普文章、相关会议信息及求职招聘等各种形式投稿。
联系邮箱:china@virology.com.cn
★