AML难治患者治疗前后基因突变的真实对比
患者信息
患者女,28岁,急性髓细胞白血病M5(急性单核细胞白血病),经MA化疗方案治疗后未缓解(NR)。化疗后白细胞计数(WBC) 1.15×109/L,血红蛋白浓度(HB) 82g/L,血小板计数(PLT) 89×109/L,原始细胞比例17%。
血液病基因检测
分别取患者初诊(1月23日)外周血样本及化疗后(3月29日)骨髓样本,于安诺优达基因科技进行基于NGS技术的血液病基因检测——安百AnnoBrightTM ,以对患者进行精确预后评估。
检测内容
安诺优达血液肿瘤综合性基因检测全面包括CEBPA、DNMT3A、FLT3等在内的111个基因,共654个编码区域,约26.1万个位点(碱基)。检测范围包括基因编码区的热点突变(SNV,InDel)和FLT3-ITD。
详细位点信息
第一次检测结果:1月31日,外周血样本
|
编号 |
位点信息 |
突变频率 |
位点意义 |
备注 |
|
1 |
NM_002520(NPM1): c.861_862insTGCA(p.L287fs) |
50.00% |
预后:单独出现NPM1突变的AML患者,预后良好 |
- |
|
2 |
NM_004119(FLT3): c.2503G>T(p.D835Y) |
45.30% |
预后:发生FLT3-TKD突变的AML患者,预后存在争议 |
- |
|
3 |
NM_001127208(TET2): c.4120T>A(p.C1374S) |
44.40% |
预后:发生TET2突变的中低危 AML患者,预后不良 |
- |
|
4 |
NM_024426(WT1): c.1144_1145insTCGG(p.A382fs) |
1.40% |
预后:发生WT1突变的AML患者,预后影响多篇研究结论不一致 |
- |
第二次检测结果:3月29日,骨髓样本
|
编号 |
位点信息 |
突变频率 |
位点意义 |
备注 |
|
1 |
NM_002520(NPM1): c.861_862insTGCA(p.L287fs) |
37.80% |
预后:单独出现NPM1突变的AML患者,预后良好 |
多基因分析:NPM1(+)/FLT3-ITD(+),AML患者预后结果更与单纯FLT3-ITD患者相似 |
|
2 |
FLT3-ITD |
/ |
预后:AML患者预后不良 |
|
|
3 |
NM_024426(WT1): c.1144_1145insTCGG(p.A382fs) |
41.00% |
预后:发生WT1突变的AML患者,预后影响多篇研究结论不一致 |
- |
突变基因解读
1. NPM1
2015年NCCN《急性髓细胞白血病临床实践指南》指出正常核型的患者出现NPM1突变,且无FLT3-ITD突变或单纯双等位基因CEBPA突变,其预后良好,属于低危组[1]。NPM1(核磷蛋白)定位于第5号染色体长臂(5q35),其所编码的蛋白是核仁颗粒区的主要蛋白之一。NPM1突变常见于AML患者,在核型正常的AML患者中的发生频率约为60%,常见于12号外显子的移码突变,以6种突变体为主(突变A-F),最常见的为A型,占70%-80%,还存在部分少见突变,如:插入GTTC、TTTG等[2,3]。
2. FLT3
2015年NCCN《急性髓细胞白血病临床实践指南》指出发生FLT3-TKD突变的AML患者,预后情况目前存在争议[1]。FLT3基因位于13号染色体长臂1区2带,编码含有993个氨基酸组成的膜结合酪氨酸激酶受体,FLT3属于Ⅲ型酪氨酸激酶受体家族成员,在调节造血细胞增殖、生存、黏附、迁移中起重要作用。在AML中FLT3突变主要有FLT3内部串联重复(FLT3-ITD)和FLT3酪氨酸激酶结构域点突变(FLT3-TKD)两种突变形式,分别约占AML的20%和7.7%[4]。
3. TET2
2015年NCCN《急性髓细胞白血病临床实践指南》指出TET2基因突变可作为评估AML预后情况的备选基因[1]。TET2基因位于4号染色体,由11个外显子组成。TET2在血液系统恶性肿瘤中的高频率突变表明TET2可能是造血的生理调节因子,它对造血分化和平衡调节起到关键作用。TET2突变在15%的髓系肿瘤中出现,突变类型多为导致蛋白截断的移码、缺失等突变[5],在原发性AML患者中TET2突变率为12%-17%,在继发性AML患
者中为19.8%-24%[6]。
4.WT1
2015年NCCN《急性髓细胞白血病临床实践指南》指出WT1基因的过表达在AML患者较常出现[1]。WT1基因主要调控造血祖细胞的沉默和粒单核细胞分化,WT1基因突变可促进原始细胞增殖同时阻滞其分化。WT1基因突变可见于7%-10%的AML患者,20%的双表型白血病和少量T-ALL患者中[7],突变主要发生在第7及第9外显子,多为移码突变和无义突变[8]。
讨论
患者经MA化疗方案治疗未达到缓解,从分子层面分析突变亚克隆发生了改变:
-
FLT3: c.2503G>T (p.D835Y)和TET2: c.4120T>A (p.C1374S)两个突变位点第一次检测时存在,但第二次检测时突变位点消失,可能是化疗药物作用已将突变克隆清除;
-
第二次检测发现FLT3-ITD突变,经回溯查证,第一次数据中确未发现低频突变,可能为用药造成的新发突变;
-
NPM1: c.861_862insTGCA (p.L287fs)和WT1: c.1144_1145insTCGG (p.A382fs)两个突变在两次检测中都存在,其中WT1的频率显著升高,可认为是对该化疗方案不敏感的难治突变。
复发/难治患者的二次分子检测对临床有一定参考意义:综合两次分子检测结果,可见患者预后从较为不良转变为更为不良,临床医生可据此调整进一步的治疗方案。
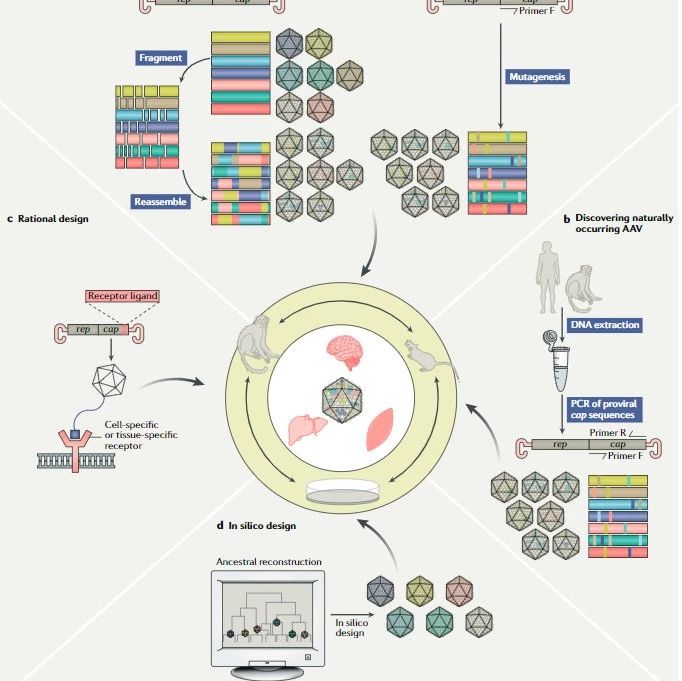
Relapse after treatment(治疗后复发模型)a.占主导的白血病克隆治疗后持续存在,成为难治、复发的克隆;b.在治疗过程中选择出少见耐药的亚克隆;c.损伤DNA的治疗药物使产生新的复发克隆;d.损伤DNA的治疗药物作用于白血病前期克隆,产生新的复发克隆。
参考文献
1. MArgaret R, Martin S, Camille N, et al. NCCN Clinical Practice Guidelines in Oncology-Acute Myeloid Leukemia–V1[R]. 2015.
2. Falini B, Mecucci C, Tiacci E, et al. Cytoplasmic nucleophosmin in acute myelogenous leukemia with a normalkaryotype[J]. N Engl J Med, 2005, 352(3): 254-66.
3. Gorello P, Cazzaniga G, Alberti F, et al. Quantitative assessment of minimal residual disease in acute myeloidleukemia carrying nucleophosmin (NPM1) gene mutations[J]. Leukemia, 2006, 20(6): 1103-1108.
4. Santos FP, Jones D, Qiao W. Prognostic value of FLT3 mutations among different cytogenetic subgroups in acutemyeloid leukemia[J]. Cancer, 2011, 117(10): 2145-2155.
5. Delhommeau F, Dupont S, Della Valle V, et al. Mutation in TET2 in myeloid cancers[J]. N Engl J Med, 2009,360(22): 2289-2301.
6. 周念, 胡建达. 成人急性髓系白血病新的基因突变与预后相关性研究进展[J]. 临床血液学杂志, 2014, 27(1):75-79.
7. Tosello V,Mansour MR,Barnes K et al. WT1 mutations in T-ALL[J]. Blood, 2009, 114(5): 1038-1045.
8. Ho PA,Zeng R,Alonzo TA,et al. Prevalence and prognostic implications of WT1 mutations in pediatric acute myeloidleukemia (AML): a report from the Children's Oncology Group[J]. Blood, 2010, 116(5): 702-710.