基因编辑系列(一):初谈基因编辑的发展史
最近一段时间,想必大家的朋友圈都被王健林的“小目标”刷屏了吧。生物界的筒子们,为了让你们充实愉快地度过这国庆假期,今天就跟小编一起定个小目标,学学基因编辑如何发家致富的吧。
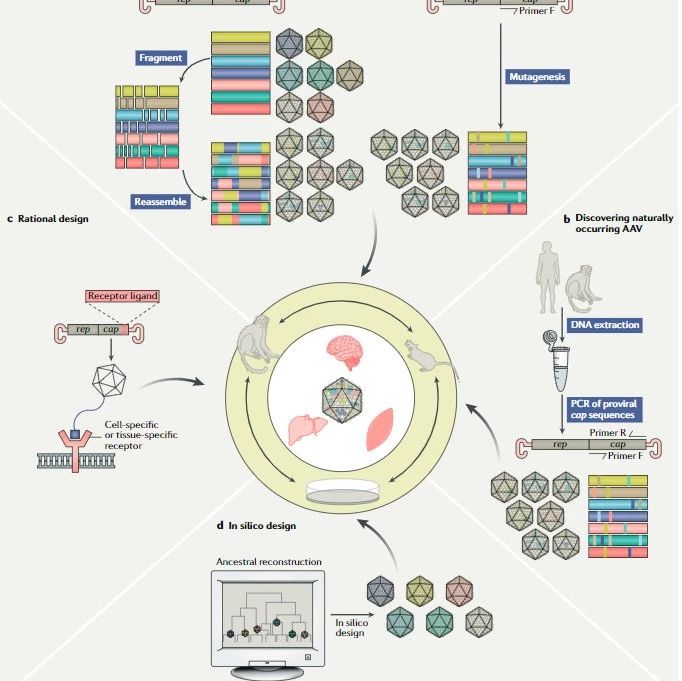
现今,基因编辑已经广泛应用于生物医学的很多领域,如疾病机理研究、基因治疗及动植物遗传育种等,不仅仅是生物领域的同行们,就连菜市场的大妈大爷都知道转基因这回事了。那所谓的基因编辑如何科学的解释,它又是如何一步步发展起来的呢?
基因编辑(gene-editing)的基本原理其实就类似word程序中的查找、替换或者删减过程,即人为地修饰宿主细胞DNA序列后,实现对特定的目的基因片段的“编辑”——敲除/敲入,从而达到改变宿主细胞的基因型的目的。
随着科学技术不断进步,基因编辑技术已经日益成熟,想要实现对基因组的编辑变得不再那么困难,特别是第三代技术CRISPR/Cas9的出现,目前被认为是最简单高效的基因编辑手段,下面小编就带着大家看看基因编辑的发展历史。
第一代技术: ZFN(锌指核酸酶)
出现时间:1996年
组成单元:识别特定的DNA序列的 ZFN +核酸内切酶FOKI
发现:锌指结构域(Zinc Finger Nucleases , ZFN)是真核生物中最为普遍的DNA结合模块
作用原理:
-
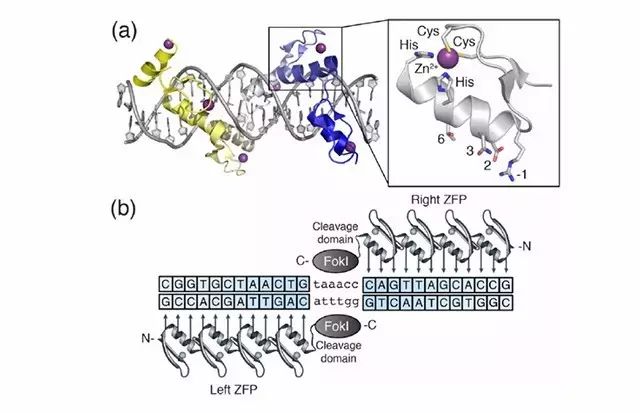
一对人工设计的,识别特异DNA序列的锌指核酸酶ZFN与目标DNA序列结合;
-
FokI核酸内切酶将形成二聚体,从而割DNA双链,形成双链断裂 ( double strand break, DSB),DNA损伤后修复会造成基因敲除或敲入等。
通过加工改造ZFN的DNA结合域,便可靶向不同的DNA序列,进行特异性切割。
ZFN的结构及作用原理图(引自文献1)
应用:
-
构建基因编辑的模式动物;
-
遗传育种;
-
基因治疗。
优点:设计比较简单,效率较高。
缺点:1. 劳动量大,周期长; 2. 成功率低易脱靶; 3. 细胞毒性大。
重大突破:Sangamo Biosciences公司基于ZFNs技术治疗艾滋病CCR5的方法已经进入临床II期试验,这是史上第一次应用基因编辑技术来治疗人类疾病。
第二代技术:TALEN(转录激活样效应因子核酸酶)
出现时间:2011年
组成单元:识别特异DNA序列的蛋白分子TALE +核酸内切酶FOKI
发现:源于黄单胞菌属(Xanthomonas)植物病原菌,它通过 III 型分泌系统将效应蛋白(TALEN(Transcription Activator-likeeffector, TAL effector))输入植物细胞质内,类似于模拟真核细胞转录因子对宿主细胞进行重编程。
作用原理:
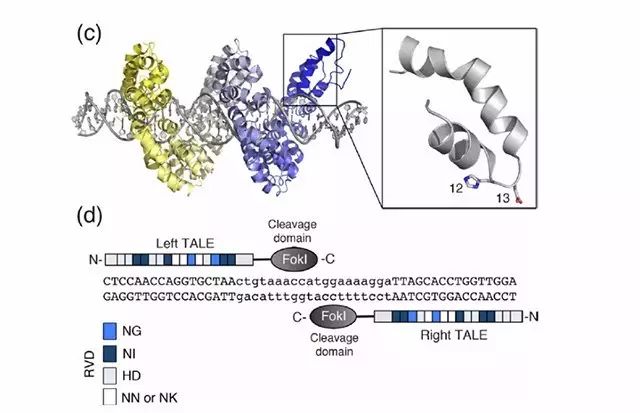
TALEN的结构及作用原理图(引自文献1)
-
人工设计识别特异DNA序列的TALEN与目标DNA序列结合;
-
FokI核酸内切酶切割DNA双链,双链断裂DNA后,损伤后修复会造成基因敲除或敲入等。
TALEN包括中间串联重复结构域,核定位信号以及酸性转录激活结构域,且高度保守。TAL效应因子对靶点的特异性是由重复模块数目和排列顺序决定的。
应用:
-
构建基因编辑的模式动物;
-
遗传育种;
-
基因治疗。
优点:平台比较成熟。
缺点:1. 依赖上下游序列;2.脱靶率较高;3. 具有细胞毒性。
重大突破:2012年的《科学》(Science)则将TALEN技术列入了年度十大科技突破;
Cellectis公司用TALEN改造的基于异源基因的CAR-T——UCART19成功缓解了Layla的不治之症–急性淋巴细胞性白血病(ALL)。
第三代技术:CRISPR/Cas9(成簇的规律性间隔的短回文重复序列)
出现时间:2013年
组成单元:成簇的规律性间隔的短回文重复序列CRISPR + 核酸内切酶Cas9
发现过程:CRISPR系统是古细菌和细菌的一种不断进化适应的免疫防御机制,早在1987年发现大肠杆菌里有串联间隔重复序列,直到2002年被命名为CRISPR(Clusteredregulatory interspaced short palindromic repeats)。2012年CRISPR/Cas9的详细作用机制被发现,并预测可作为基因编辑技术。
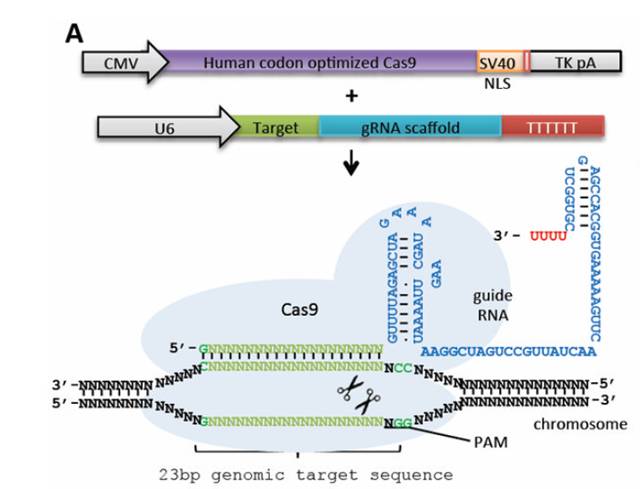
作用原理:人工设计的gRNA( guide RNA)来识别目的基因组序列,并引导Cas9蛋白酶进行有效切割DNA双链,形成双链断裂,损伤后修复会造成基因敲除或敲入等。
应用:
-
构建基因编辑的模式动物;
-
遗传育种;
-
基因治疗。
优点:较前两代技术更加高效、快捷、准确、廉价。
缺点:1. 有局限性,靶序列前无PAM序列不能切割;2. 仍存在一定的脱靶效应。
重大突破:已成立多家CRISPR相关公司,致力于用来治疗基因遗传病,已在很多疾病取得较好临床前效果。
CRISPR/Cas9系统组成及作用原理图(引自文献2)
以上三种技术的共同点:切割DNA后造成的损伤及修复过程
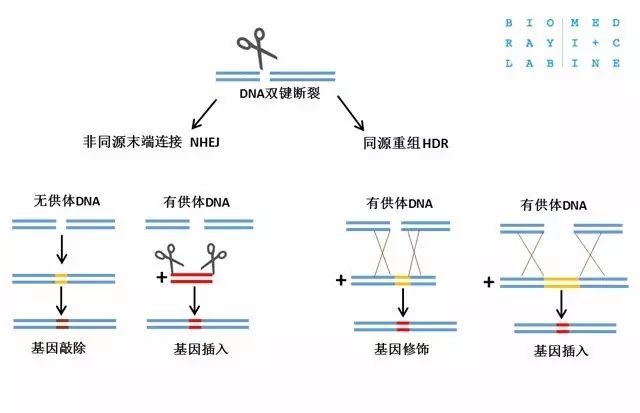
DNA链断裂后,主要通过易错性的非同源末端连接(Non -homologous end joining, NHEJ)以及高保真性的同源重组(homologous recombination, HR)进行修复,最终会造成基因敲入(knock in)、敲除(knock out)、缺失(deletion)及基因修饰(gene modification)这几种类型。
DNA损伤后介导的修复途径(引自文献3)
基因编辑看似很高大上,又很深奥的知识,其实大家用心地经历本次的学习后,相当于已经迈向了很大一步了。总结一下,基因编辑技术至此已经发展到第三代,一代比一代高效快捷,陆续也一直有新技术出现,相信编辑基因组DNA会更加简单。
参考文献
Thomas Gaj, Charles A. Gersbach, and Carlos F. Barbas III.(2013) ZFN, TALEN, and CRISPR/Cas-based methods for genome engineering. Trendsin Biotechnology, 31(7): 397-405.
DiCarlo, Julie E. Norville1, George M. Church. (2013)RNA-guided human genome engineering via Cas9. Science, 339(6121): 823-826.
Tomoji Mashimo. (2014) Gene targeting technologies inrats: Zinc finger nucleases, transcription activator-like effector nucleases,and clustered regularly interspaced short palindromic repeats. DevelopmentGrowth Differentiation, 56(1): 46–52.